京都大学:新型熔融KOH-水体系高温碱水电解
为了提高水电解效率,我们研究了高温(150℃)下镍电极在熔融KOH-H2O体系(85:15wt%,65:35mol%)中的析氢和析氧反应(HER和OER)。在500 mA*cm-2下,与传统水溶液(30wt% KOH, 80℃)相比,新型体系中HER和OER的过电位分别显著降低了261mV和75mV。极化的减少主要归因于动力学效应,包括速率决定步骤的变化,并随着电解质的变化对HER和OER产生影响。
研究背景
传统的商业水电解包括碱性水电解(AWE)。AWE可以采用廉价的材料,如Ni作为电极材料,这允许大规模的电解槽;然而,由于电极反应中存在较大的过电位和欧姆损耗,在高电流密度下难以实现。因此,高效率和高电流密度对AWE至关重要。一般来说,水电解制氢所需的能量消耗主要由电解槽的电压决定。降低电压是提高效率的必要条件,降低析氢反应(HER)和析氧反应(OER)的过电位至关重要。传统的商业AWE使用20-30wt%KOH水溶液,电解温度为60℃-80℃提高电解温度是降低HER和OER过电位的有效途径。以前的研究报告了高温范围(高于100℃)至400℃使用30-52wt%KOH水溶液的结果。之前的高温实验都是用KOH水溶液在加压条件下抑制水分蒸发进行的。在这项研究中,我们重点研究了熔融KOH-H2O体系(85:15wt%,65:35mol%)中的水电解,这是一种超浓的KOH溶液,以前没有报道过。根据公布的数据,85%KOH体系的熔点为100.4℃(图1),沸点估计超过300℃。采用线性扫描伏安法(LSV)和恒流电解法研究了镍电极在高温150℃和常压下的KOH-H2O(85wt% KOH)熔融体系中的HER和OER行为,并将结果与传统的30wt%KOH水溶液在80℃下的结果进行了比较。
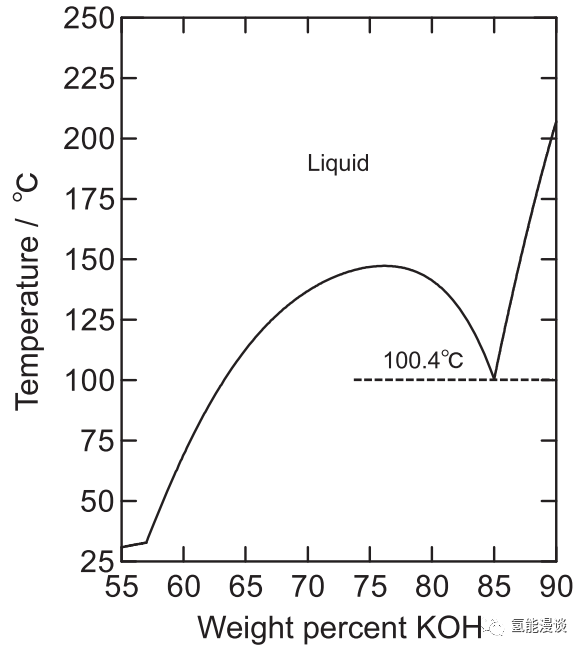
图1 KOH和H2O体系二元相图
用LSV在Ni电极上进行极化测量,扫描速率为10mV*s-1。在150℃的KOH-H2O溶液中,HER和OER的极化比在80℃的30wt% KOH水溶液中明显降低。
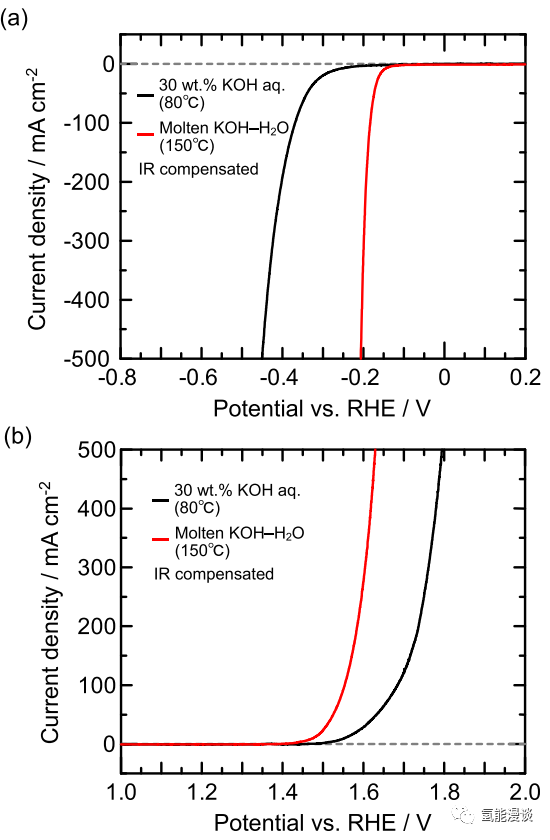
图2 HER与OER的LSV
图3显示了由lsv构建的Tafel图。在水溶液KOH中,HER的Tafel斜率为-100mV*dec-1,而在熔融KOH- H2O中的Tafel斜率要低得多,为-34mV dec-1。对于OER,水溶液中KOH的Tafel斜率为87mV*dec-1,熔融KOH- H2O的Tafel斜率为72 mV*dec-1,比水溶液低15mV*dec-1。在塔菲尔地区也观察到这种变化。在KOH水溶液中,Tafel区为10-200mA*cm-2,在KOH-H2O熔融溶液中,Tafel区为5-1500mA*cm-2,向高电流密度范围显著扩展。同样,对于OER,水溶液KOH中的Tafel区为3-30mA*cm-2,熔融KOH-H2O中的Tafel区为3-70mA*cm-2,表明Tafel区扩展到高电流密度范围。Tafel斜率随电解液从KOH水溶液到KOH-H2O熔融的变化而减小,这表明HER和OER的速率决定步骤发生了变化。塔菲尔区扩大到高电流密度范围也被认为促进了传质。这些影响在HER中比在OER中更为显著。这些结果表明,速率决定步骤的变化与传质的促进有关。电解液由水溶液KOH变为熔融KOH-H2O是导致HER和OER极化降低的主要原因。
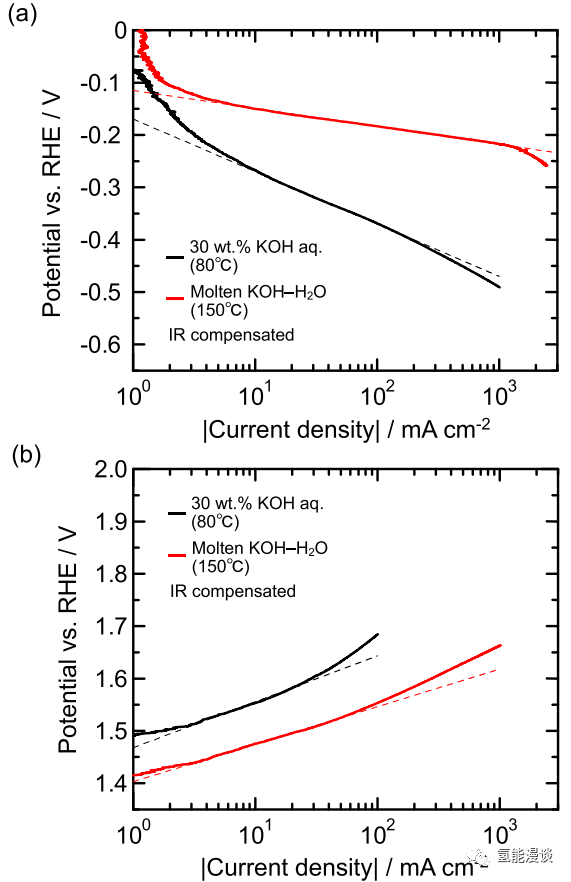
图3 (a)HER,(b)OER的塔菲尔斜率
在±500 mA cm-2(相当于传统商用AWE的高电流密度)和±1000mAcm-2(相当于电流密度的两倍)下进行恒流电解,以测量稳态电位。图4显示了水溶液KOH和熔融KOH-H2O的过电位变化。与LSV的结果相似,随着电解质从水溶液KOH变为熔融KOH-H2O,HER和OER的过电位显著降低。具体来说,在500 mA*cm-2时,HER过电位从467mV(水溶液KOH)降低到206mV(熔融KOH-H2O),降低261mV。OER过电位从553mV(水相KOH)降低到478mV(熔融KOH- H2O),降低了75mV。因此,总过电位降低了336mV,从1020mV(水态KOH)降低到684mV(熔融KOH-H2O)。这里,当温度从80℃升高到150℃时,标准理论分解电压降低了28mV。由上述数值可知,当电解液由KOH水溶液变为KOH-H2O熔融时,总过电位和标准理论分解电压降低了364mV。因此,热力学效应对极化降低的影响为8%,而动力学效应为92%,表明极化随电解质的变化而降低主要是由于动力学效应。如图4所示,即使电流密度从500 mA*cm-2增加到1000mA*cm-2,总的过电位降低了361mV,从1149mV(水溶液)降至788mV(熔融KOH-H2O)。这些结果表明,即使在比传统AWE更高的电流密度下,使用熔融KOH-H2O系统进行水电解也有可能提高能源效率。
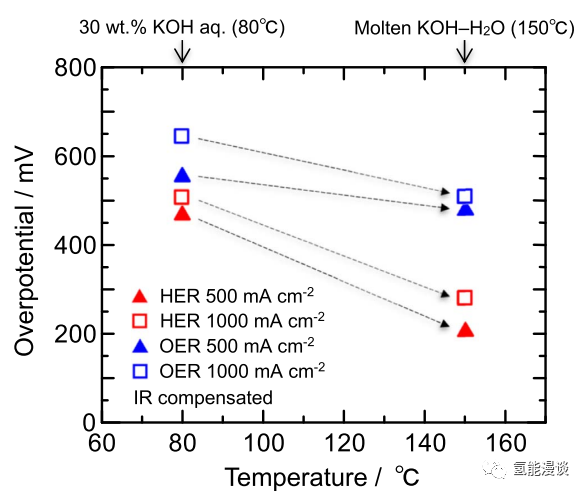
图4 Ni电极HER与OER过电势改变
结论
在这项研究中,为了开发高效的水电解,我们研究了镍电极在高温150℃的熔融KOH- H2O体系(85wt% KOH)中的HER和OER行为。在LSV中,与传统体系(30wt%KOH水溶液,80℃)相比,新型体系中Ni电极上的HER和OER的极化明显降低。Tafel图显示,电解液从水溶液KOH转变为熔融KOH-H2O导致的速率决定步骤的改变和传质的促进是降低HER和OER极化的两个主要因素。在±500mA*cm-2的恒流电解过程中测量稳态电位,这与传统商用AWE的高电流密度相对应。结果表明,随着电解质的改变,HER过电位降低261mV, OER过电位降低75mV,共降低336mV。80℃时的KOH水溶液和150℃时的KOH- H2O熔融之间极化减小的热力学效应为8%,而动力学效应为92%,说明随着电解质的改变,极化减小,主要是由于动力学效应。即使电流密度从500mA*cm-2增加到1000mA*cm-2,总过电位也降低了361mV。




